涉水产品卫生许可批件

西安华道安创信息技术有限公司
全国免费咨询电话:4006-010-725
总部:西安市未央区未央路80号
139-0928-9277
北京:海淀西三环昌运宫紫竹桥
136-8120-0268
上海:闵行区光华路18号
152-2175-9315
青岛:市南区中山路10号
137-9194-1216
杭州:滨江区伟业路1号
158-6716-8335
深圳:南山区粤海街道环东路西环北路北滨海之窗花园
130-7782-9315
QQ:3568192523
网址:http://www.xahdgw.com
邮箱:hdzygw#126.com(#换@)
您现在的位置:网站首页 >涉水产品卫生许可批件 >消毒产品检测报告_消毒剂_消毒设备(器械)_生物(化学)指示物_一次性 卫生用品_消毒产品检测机构消毒产品检测报告_消毒剂_消毒设备(器械)_生物(化学)指示物_一次性 卫生用品_消毒产品检测机构
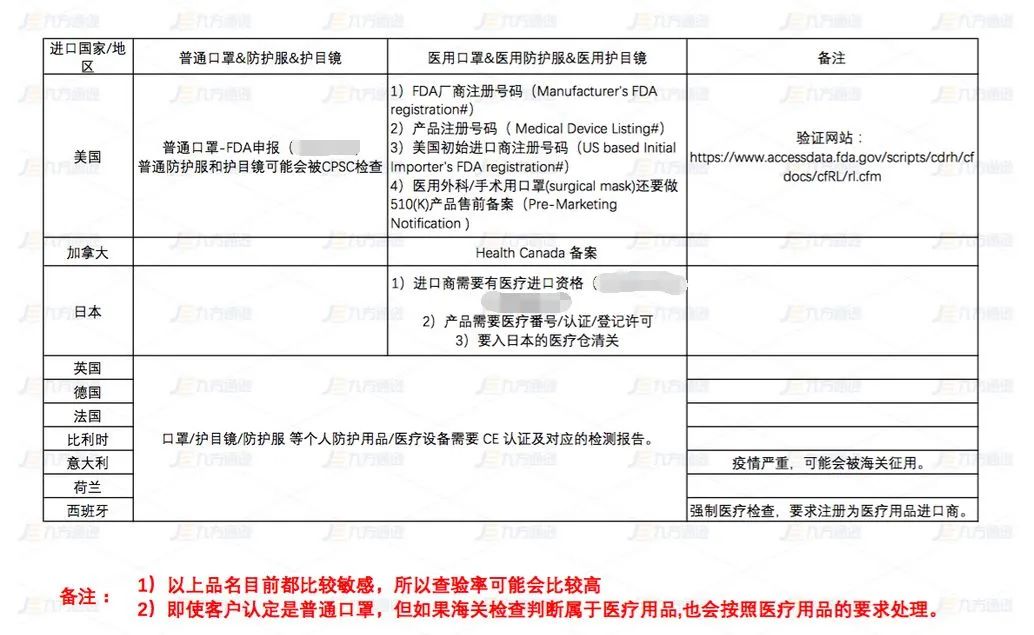
出口口罩需具备哪些资质?各国检测标准及认证要求
文章来源:跨境电商与创业文摘 编辑:西安华道安创
日本、韩国、美国、意大利、伊朗、巴基斯坦、西班牙等国也受疫情影响,出现了口罩短缺,或限制口罩供应的情况。现在很多地区都存在着口罩供不应求的局面,以下针对口罩等疫情物资的进出口问题,收集和整理了一些要求和规范,希望能帮助到疫情物资进出口企业。
疫情物资商品编码参考:
|
急需物资
|
参考税号
|
|
口罩
|
|
|
橡胶手套
|
|
|
防护服
|
|
|
护目镜
|
|
|
棉签、棉棒、棉球
|
|
|
体温计
|
|
|
消毒液
|
|
|
洗手液
|
中国出口(公司行为)
用于销售
需要经营范围内有医疗器械经营许可证的,进出口权的,才能出口。
用于赠送或代为采购
作为赠送的,或者代关联公司(兄弟公司,母子公司)采购的,要提供采购的厂家或公司的国内生产厂家的相关资质证明文件,与我们进口时要国外提供三证(营业执照,产品医疗器械备案证明,厂家检查报告)一个道理。
韩国
必要资料(资质)
提单,箱单,发票,韩国进口商营业执照,韩国收货人需要到韩国药监局Korea Pharmaceutical Traders Association. 提前备案进口资质(没有不行)网址:www.kpta.or.kr。
企业自用又是受赠的情况,可以自行进口,不需要有相关资质。
口罩要求
口罩还需要有详细的原产地标识,如果是中国制造务必有标签:Made in China, 生产厂家信息,保质期,还要准备成分含量说明,制造工艺流程,这些文件都有了还没有结束,还需要货物到了韩国以后进行精监化验送交样品到实验室,化验合格后方可进入韩国市场销售流通。
日本
必要资料(资质)
提单,箱单,发票
出口日本的PMDA注册医疗器械公司希望把产品投放到日本市场必须要满足日本的Pharmaceutical and Medical Device Act (PMD Act),在PMD Act的要求下,TOROKU注册系统要求国外的制造商必须向PMDA注册制造商信息。
口罩要求
包装上印有ウィルスカット99%的字样都是超过国内过滤效率95%(N95口罩)标准的医用口罩!
PFE:0.1um微粒子颗粒过滤效率
BFE:细菌过滤率
VFE:病毒过滤 率
ウィルスカット:病毒拦截
1. 医用防护口罩:符合中国GB 19083-2010 强制性标准,过滤效率≥95%(使用非油性颗粒物测试)。
2. N95口罩:美国NIOSH认证,非油性颗粒物过滤效率≥95%。
3. KN95口罩:符合中国GB 2626 强制性标准,非油性颗粒物过滤效率≥95%
欧盟
必要资料(资质)
提单,箱单,发票
口罩要求
在欧盟,口罩属于PPE个人防护用品,“危及健康的物质和混合物”。2019年起,欧盟新法规PPE Regulation (EU) 2016/425强制执行,所有出口欧盟的口罩必须在新法规的要求下获得CE认证证书。
CE认证是欧盟实行的强制性产品安全认证制度,目的是为了保障欧盟国家人民的生命财产安全。
美国
必要资料(资质)
提单,箱单,发票
美国进口的口罩,若需要销售,必须要拿到FDA认证才可以在美国本土市场进行销售活动。对于自用和赠送的口罩,大家在出口的时候最好先问一下美国接收方面,是否也需要FDA认证,或者采购原本就通过FDA认证的口罩进行出口。
口罩要求
根据HHS(美国卫生及公共服务部)法规,NIOSH(美国国家职业安全卫生研究所)将其认证的防颗粒物口罩分为9类。具体的认证则由NIOSH下属的NPPTL 实验室操作。
在美国,按过滤网材质的最低过滤效率,可将口罩分为三种等级——N ,R ,P。
N类的口罩只能过滤非油性颗粒物,比如:粉尘、酸雾、漆雾、微生物等。空气污染中的悬浮微粒,也多是非油性的。
R口罩只适合过滤油性颗粒物及非油性颗粒物,但用于油性颗粒物时限制使用时间不得超过8小时。
P类口罩则既可过滤非油性颗粒物,又可过滤油性颗粒物。油性颗粒物比如:油烟、油雾等。
根据过滤效率的不同,又有90,95,100 的差别,分别指在标准规定的测试条件下最低过滤效率为90%,95%,99.97%。
N95不是特定的产品名称。只要符合N95标准,并且通过NIOSH审查的产品就可以称为“N95型口罩”。
澳大利亚
必要资料(资质)
提单,箱单,发票
口罩要求
AS/NZS 1716:2012是澳大利亚和新西兰的呼吸保护装置标准,相关产品制造流程和测试必须符合本规范。
该标准规定了防颗粒口罩制造过程中必须使用的程序和材料,以及确定的测试和性能结果,以确保其使用安全。
个人行邮方式
1. 由于每个国家关于进口口罩的要求不同,建议大家出口前务必咨询当地的代理公司或者接收方,避免物资被扣或者被退回的问题。
2. 自用口罩的出口以及快递,数量一定要在合理范围,如果数量巨大也有可能被国外海关扣押。
3. 目前航空海运运力还没有完全恢复,运输时间都相对较长,建议在发货后留意单号更新,同时耐心等待,只要没有违规问题,一般不会被扣押或者退回。
再次提醒:
目前并没有官方禁止口罩出口的消息。建议中国卖家及时关注国内外防疫物资出口资质认证和监管要求,避免造成产品被扣押和退回的风险。属于医疗器械类的口罩,不同国家的资质和要求都不相同,这点卖家们一定要注意。
国内外销售都需要先获得《第二类医疗器械经营备案凭证》,若想在 跨境平台销售,除了类目审核,还需要产品认证,欧美必须通过当地国家认证许可,如欧盟CE认证,美国NIOSH认证。欧盟CE认证还需要注意包装、质量符合要求,要有欧洲代理信息。并最好保留好认证证书,采购发票或原材料发票。
目前国内疫情趋于缓和,欧洲、意大利、日本、韩国等感染人数持续上升,伊朗以极高的致死率引发全球关注。鉴于此,口罩商机很快转移到了国外,口罩出口,成为如今疫情下的热门生意。
美国口罩标准及认证要求
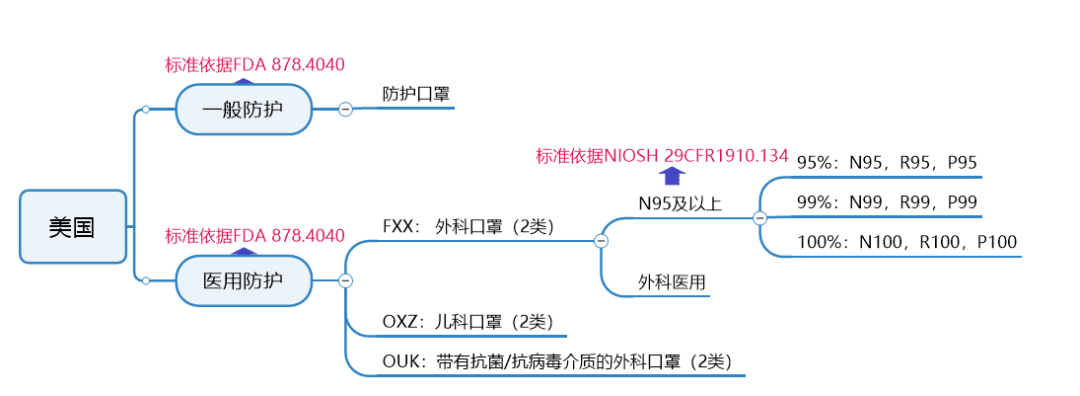
美国一般防护口罩认证要求:
按照美国FDA医疗I类做认证,流程为:
①填写申请表格,信息确认;
②获取PIN码,交付年费;
③下发注册号;
④产品出口。
美国医用外科口罩认证要求:
按照美国FDA医疗II类做认证,流程为:
①产品测试(性能测试、生物学测试);
②准备510K文件,提交FDA评审;
③FDA发510K批准信;
④完成工厂注册和机器列名;
⑤产品出口。
美国医用N95及以上9种口罩认证要求:
按照NIOSH认证标准,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系部分资料)至NIOSH文审,文审和测试都通过后,NIOSH核发批文。
欧盟口罩标准及认证要求
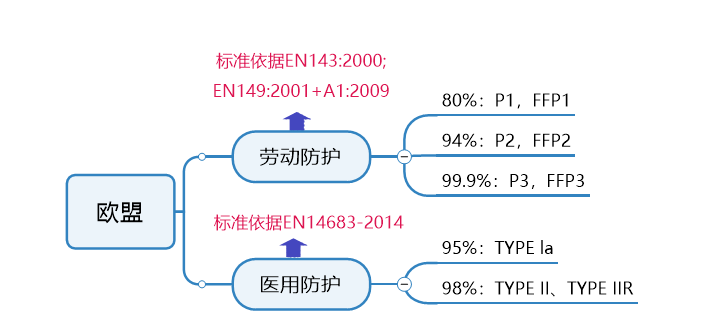
欧盟一般防护口罩认证要求:
个人防护口罩的欧洲标准是EN149及EN143,防护口罩需要满足欧盟个人防护设备指令(PPE)的要求,审核企业质量管理体系和CE技术文档,审核通过后可获得PPE法规的CE证书。
欧盟医用防护口罩认证要求:
医用口罩对应的欧洲标准是EN14683,按照医疗器械法规2017/745/EU的要求,口罩产品可以按照一类器械进行管理。依据产品是无菌或非无菌状态提供,认证模式有所差别。
澳大利亚&新西兰口罩标准及认证要求
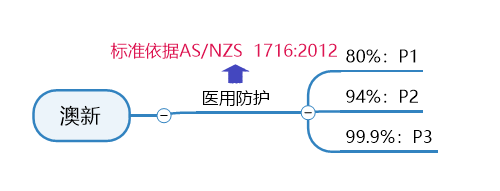
澳新医用防护口罩认证要求:
AS/NZS1716:2012是澳大利亚和新西兰的呼吸保护装置标准。该标准规定了防颗粒口罩制造过程中必须使用的程序和材料,以及确定的测试和性能结果,以确保其使用安全。
韩国口罩标准及认证要求
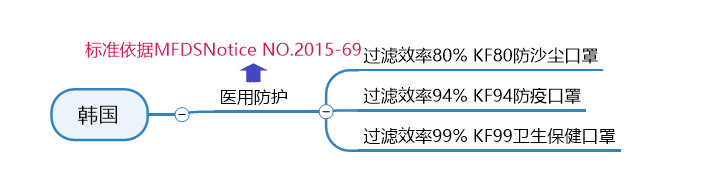
韩国医用口罩认证标准:
韩国的口罩标准KF (Korean filter) 系列,是由韩国的食品药品管理部门 (Ministry of Food and Drug Safety,MFDS) 发布的韩国主流口罩标准 (Regulations on the Approval,Notification,and Evaluation of Quasi-Drugs) 。
日本口罩标准及认证要求
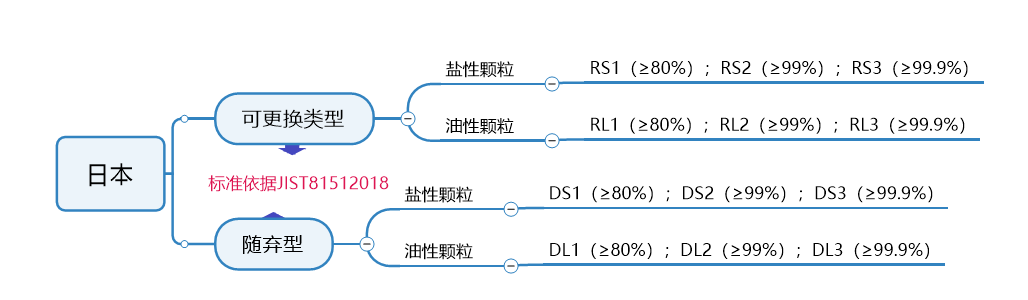
以上内容仅供参考,请以实际业务为准!
【返回 】
